消瘦综合症恶病质的难以捉摸的机制揭示
土耳其科克大学分子生物学和遗传学系以及比利时鲁汶大学实验和临床研究所内分泌学、糖尿病学和营养学的研究人员合作研究了与癌症相关的消瘦背后的机制综合征——恶病质。
发表在《自然》杂志上的论文“EDA2R–NIK信号促进与癌症恶病质相关的肌肉萎缩”详细介绍了外发育不良蛋白A(EDA)的可变剪接如何导致恶病质病理学中的信号通路的发现。在同一期刊上发表的一篇新闻与观点文章概述了这项研究的发现。
EDA是一种细胞因子,属于肿瘤坏死因子(TNF)信号蛋白超家族,由白细胞产生以完成免疫系统的工作。研究人员发现,EDA的另一种剪接,即EDA2R信使RNA,在患有消瘦综合征恶病质小鼠的骨骼肌组织中富集。
消瘦综合症
恶病质最常出现在晚期胰腺癌和肺癌中,也常见于结直肠癌、卵巢癌和肝癌。
恶病质定义为在过去六个月内体重减轻5%或更多,恶病质还会导致疲劳和力量下降。这个定义本身就是对更复杂的生理状况的粗略衡量,在诊断中可能会被遗漏,因为它与癌症治疗可能产生的类似效果重叠。
由于缺乏体力或缺乏食欲,患者可能无法执行日常任务,如洗澡、购物或自己进食,恶病质导致的身体萎缩会加速。心理健康问题很快就会随之而来。此外,当肌肉损失导致心脏或呼吸衰竭时,恶病质的后果被认为是近三分之一癌症死亡的直接原因。
如果没有已知的机制,即使是诊断在没有有效治疗和明确行动方案的情况下在临床环境中的使用也可能受到限制。
有趣的相关性
通过肌肉活检中的基因表达搜索,研究人员检测到与没有恶病质和无癌症对照的癌症患者相比,恶病质癌(肺癌、胃肠道癌、胰腺癌和结直肠癌)患者的EDA2RmRNA升高。
此外,研究小组发现患有肌肉质量和功能下降的杜氏肌营养不良症(DMD)和面肩肱型肌营养不良症(FSHD)患者的EDA2R转录本也显着升高。
随着检测到EDA-A2-EDA2R通路相关性,研究人员进一步开展了调查。
发现机制
从组织培养开始,然后发展到小鼠模型,该团队反复发现增强的EDA-A2蛋白水平会产生有害影响。他们观察到组织培养物中的细胞变小,体内小鼠实验显示肌肉严重退化。
实验还揭示了EDA-A2在与其受体相互作用后的下游效应。NFĸB诱导激酶(NIK)是控制大量基因表达的转录因子的关键调节因子,它启动以激活转录可分解肌肉组织的酶的基因。
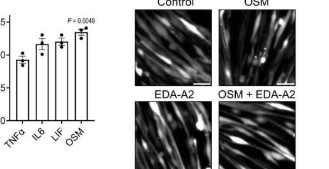
在受体EDA2R表达的上游,研究人员将肿瘤诱导的制瘤素M(OSM)确定为关键的上调调节剂。肌肉中OSM信使RNA的耗尽保护它们免于消瘦和萎缩。
研究结果表明,OSM–OSMR信号与EDA2R–NIK通路并行作用,并加强肌肉萎缩和EDA2R上调。
在小鼠中删除EDA2R或NIK足以赋予对肿瘤诱导的肌肉萎缩的抵抗力。作者建议靶向OSM-OSMR通路也可能是一个高价值的治疗靶点。
与任何好的研究结束一样,还需要进行更多的研究。接下来的步骤可能是确定哪些目标具有最佳的风险收益比,并推进对临床干预因果关系的理解。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。










