神经科学工具的结构可能会导致下一代版本
为了更全面地了解疾病是如何在大脑中产生的,科学家们必须阐明神经元沿着复杂的神经细胞网络传递信息(化学或电)的复杂方式。一种方法是使用称为DREADDs的工具,它代表由设计师D地毯激活的设计师受体A。
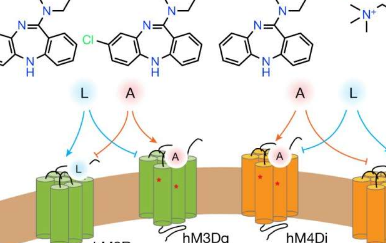
当引入神经细胞或神经元时,DREADDs就像一把专门的锁,只有当一把钥匙——以合成设计师药物的形式——插入那把锁时,它才会起作用。DREADDs可以让研究人员打开或关闭特定的细胞功能,以更精确地检查电路中的神经元组。(见动画)
现在,马里兰大学医学院的一名研究员和他在北卡罗来纳大学教堂山分校(UNC)的同事揭示了这些DREADD的结构,这将为创建下一代这些工具铺平道路。这一步最终将使他们更接近一个难以实现的目标——了解精神分裂症、药物滥用、癫痫和阿尔茨海默氏症等脑部疾病的基础,以便开发更有效的药物来治疗它们。
研究小组在最近一期的《自然》杂志上发表了他们的发现。
研究作者、生物化学助理教授JonathanFay博士说:“这些发现为药物结合的DREADD受体的性质提供了原子清晰度,这是所有这些技术在正确的地点和正确的时间融合的结果。”和UMSOM的分子生物学。“这些知识将使这个工具得到进一步完善和优化。我们以前在如何升级他们的设计方面受到限制,因为我们不完全了解他们在结构层面的工作方式。”
全世界数百个实验室现在使用由UNC开发的DREADD工具。那里的科学家设计了这些受体蛋白,使其仅与独特设计的药物发生反应,这些药物具有药理学惰性,因为它们仅与DREADD蛋白受体结合。
对于这项新研究,研究人员使用了一种称为低温电子显微镜的较新成像技术来确定DREADD受体与药物的分子结构。这个过程以不形成传统冰晶的方式快速冻结DREADD,而是产生一种允许分子运动的浆液。当其他较旧的分子成像方法失败时,这项技术使研究人员能够确定DREADD的结构。研究人员观察到抑制性(关闭细胞功能)或刺激性(开启细胞功能)DREADD受体与两种不同的设计药物中的每一种结合。
研究人员还比较了产生DREADD的天然大脑受体的结构,以了解它与DREADD的不同之处。在神经元细胞膜中发现的原始大脑受体传统上与参与学习和记忆的分子结合。通过改变天然受体的两个组成部分,经过改造的DREADD受体与其实验室设计的药物结合得更好,而不是与原始记忆分子结合——这是他们通过实验可视化的过程。
“通过这种成像技术,我们可以看到DREADD中的基因变化打开了记忆分子通常结合的空间,让新设计的药物滑入。我们可以看到空间的形状也发生了变化,有助于为什么新药更适合,”Fay博士说。
DREADDs起源的受体类别通常是许多治疗的预期目标。然而,各种药物会与几种受体结合或以意想不到的方式激活其他受体。结果可能是有益的,但也可能导致副作用。
UMSOM说:“由于DREADD中这些设计药物的精确结合方式如此特异,研究人员很可能有一天最终会针对许多其他类似受体开发出靶向疗法,而不会产生交叉反应和令人不快的副作用。”院长MarkT.Gladwin,医学博士,马里兰大学巴尔的摩分校医学事务副校长,JohnZ.andAkikoK.Bowers特聘教授。
虽然这项研究的显微镜相关部分发生在北卡罗来纳大学,但UMSOM在其生物分子治疗中心(CBT)也拥有高科技结构生物学能力,研究人员在那里确定人体蛋白质的结构,以更好地开发新药来治疗各种疾病。Fay博士计划使用CBT的设施来分析其他大脑受体的结构,并继续与UNC合作开发潜在的DREADD2.0版本。
马里兰大学医学神经科学研究所(UM-MIND)将于2022年底启动,证明UMSOM的研究重点包括神经科学和脑相关疾病。Fay博士的工作直接有助于实现这些机构优先事项。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。










